Puisque cet examen demeure toujours aussi usité par les différentes autorités administratives il devient nécessaire de revenir (*) sur le principe de cette technologie pour mieux en comprendre son utilisation… politique. C’est le Docteur Philippe Pognonec (**), chercheur CNRS, qui a accepté de nous en expliquer le principe et nous l’en remercions chaleureusement. Comment est-il possible qu’un innocent test de laboratoire puisse se transformer en instrument de peur et d’aliénation de nos libertés individuelles comme collectives ? C’est (presque) très simple et c’est ici, bonne lecture.
Principe de la technique de PCR
La technique de PCR, pour « Polymerase Chain Reaction » a été développée il y a plus de 35 ans principalement par Kary B. Mullis et Randall K. Saiki (1). Ce fut une avancée majeure dans le domaine de la biologie moléculaire, offrant aux chercheurs des quantités d’ADN jusque là inimaginables.
Ceci a grandement simplifié de nombreuses autres techniques, tels le séquençage nucléotidique sans clonage préalable, l’insertion rapide de modifications de séquences, et… le dosage précis de la quantité de molécules d’ADN présentes dans un échantillon inconnu.
Ceci est aujourd’hui utilisé quotidiennement pour les tests « COVID-19 », l’échantillon à analyser étant ce que l’on récupère dans la cavité naso-pharyngée à l’aide d’un écouvillon. Il serait cependant plus précis de dire « tests SARS-CoV-2 », le SARS-CoV-2 étant le virus responsable de la COVID-19. Nous y reviendrons plus loin.
Le principe général de la PCR repose sur le fait que la molécule d’ADN consiste en deux chaînes dites « complémentaires », orientées de façons opposées. Par convention, on oriente ces chaînes selon leurs extrémités, dites 5’ et 3’. L’ADN est l’enchaînement de quatre unités de base, appelées « nucléotides », ou « bases », et identifiées avec les lettres A, T, C et G. Ces enchaînements constituent un brin dADN. Un A sur un brin sera toujours face (on dit : « apparié ») à un T sur le brin complémentaire, et un C sera toujours apparié à un G. Imaginons la séquence suivante pour l’un des deux brins d’ADN : GACATTCGGA
Ce brin d’ADN se lit par convention de 5’ en 3’. Son brin complémentaire est indiqué en dessous, mais son orientation étant opposée, on le lira de droite à gauche.
Soit au final notre molécule d’ADN double brin:

Qui est constituée des deux brins complémentaires 5’GACATTCGGA 3’ et 5’TCCGAATGTC 3’ mais ceci n’est qu’un exemple simple:
Dans la vraie vie, les molécules d’ADN peuvent atteindre des longueurs gigantesques. Le chromosome humain le plus long fait 260 millions de bases, en 2 brins complémentaires, soit 520 millions de nucléotides ! (2)
Ici, pour faciliter l’explication, nous utiliserons un petit fragment d’ADN de 10 paires de bases (pb) et des amorces de 3 bases. En réalité, les PCR fonctionnent de façon optimale sur des ADN de l’ordre de 100 à 150pb, avec des amorces de l’ordre de 20 bases, spécifiques de la séquence à amplifier. La Figure ci-dessous résume ce principe :
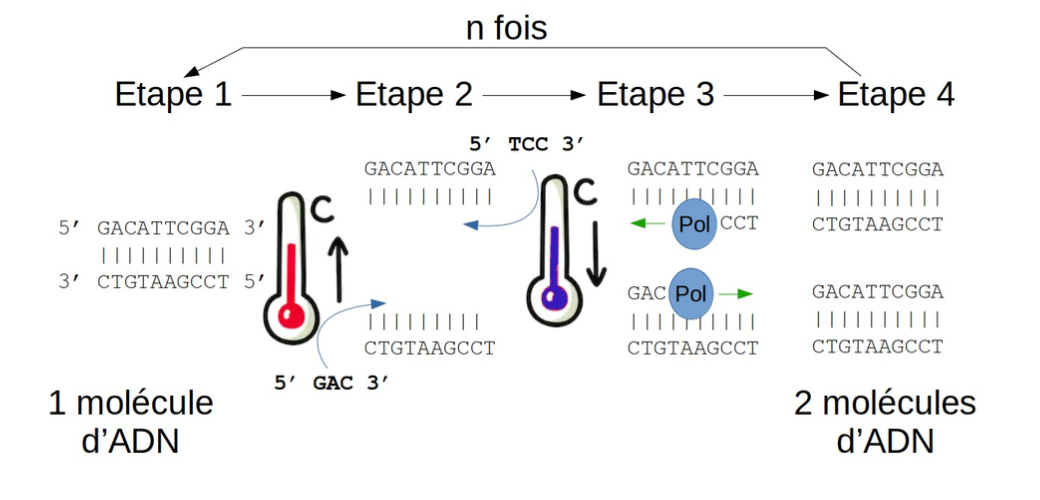
Dans l’étape 1, notre molécule d’ADN double brin (qui est la structure classique de l’ADN) représentée à gauche est chauffée à environ 90°C. Les liaisons entre les deux brins se déstabilisent, et ils se séparent (étape 2). En présence de deux petits ADN simples brins, appelés « amorces » (3 lettres en gras sur la figure), qui sont soigneusement choisis pour être complémentaires aux extrémités 5’ des deux brins, on va observer un appariement entre les brins d’ADN et ces amorces, présentes en bien plus grandes quantités (étape 3). Dès ces appariements formés, la polymérase (« Pol ») va venir se fixer aux extrémités 3’ libres des amorces, et allonger ces amorces en recréant le brin complémentaire, grâce aux nucléotides libres présents dans le tube de réaction qui viennent s’enchaîner pour « remplir » l’ADN. Finalement (étape 4), on se trouve en présence de 2 molécules complètes d’ADN double brins, qui sont les copies conformes de celle de départ. Ces quatre étapes sont ensuite répétées en cycle.
On peut calculer avec précision le facteur d’amplification que l’on obtiendra à partir de l’ADN initial : En 1 cycle, l’amplification est de 2 fois (on peut aussi écrire : 2¹)
en 2 cycles, l’amplification est de 4 fois (soit 2²)
en 3 cycles, l’amplification est de 8 fois (2³)
en « n » cycles : l’amplification est de 2n fois
Si n= 30, on aura amplifié le matériel de départ 230 fois, c’est à dire… 1.073.741.824 de fois, soit plus d’un milliard de fois !!!!
Adaptation à l’amplification d’un ARN messager
Nous venons de présenter l’amplification d’un fragment d’ADN. Le génome du SARS-Cov-2, virus responsable de la maladie COVID-19, ne peut cependant pas être amplifié directement par PCR. En effet, ce virus dispose d’un génome particulier, constitué d’ARN.
L’ARN est une structure cousine de l’ADN dans laquelle la base « T » est remplacée par « U », et l’ARN est ici présent sous forme d’un seul brin (ce qui, contrairement à l’ADN, est le cas général pour l’ARN).
Afin de pouvoir effectuer une amplification PCR à partir de ce génome ARN simple brin, une première étape est nécessaire : le passage de l’ARN en ADN (illustré sur la figure suivante). Ceci se fait en utilisant également une amorce ADN soigneusement choisie et complémentaire à l’ARN viral. Cette amorce ADN est parfaitement capable de s’apparier à son complément sur l’ARN, tout comme elle le fait sur un brin d’ADN. On ajoute à l’amorce ADN et à la matrice ARN une Polymérase particulière qui à la capacité de synthétiser un ADN complémentaire à l’ARN viral à partir de l’amorce ADN.
Cette Polymérase est nommée « Transcriptase Inverse, ou RT-Pol ». Ici, pas besoin d’amplification : on se contente d’un seul cycle de polymérisation, ou plutôt, de « rétro-polymérisation ». C’est ce fragment d’ADN simple brin nouvellement synthétisé qui servira de matrice initiale lors de la PCR, qui se déroulera exactement comme décrit plus haut.

Principe du suivi en « temps réel » de la réaction en chaîne (qRT-PCR)
Nous savons désormais préparer un ADN simple brin complémentaire à celui du génome du SARS-CoV-2 grâce à la RT-Pol, et nous savons amplifier cette matrice ADN grâce à la PCR. Mais comment utiliser la puissance de ces techniques d’amplification? Dans le cas présent, ce qui nous intéresse est de savoir « si l’on est positif ou non ». En d’autre terme, mon écouvillon contient-il de l’ARN de virus SARS-CoV-2?
Pour le savoir, on génère à chaque synthèse d’ADN un signal invariable et facilement mesurable. Plusieurs procédés le permettent. Si par exemple on génère une quantité précise de lumière à chaque création d’un brin d’ADN, il sera possible en mesurant la quantité totale de lumière produite au cours des cycles de suivre l’amplification en temps réel (Real Time, ou RT) de façon quantitative (q), et ainsi de connaître le nombre exact de molécules d’ADN synthétisées. D’où le nom de qRT-PCR.
Un moyen très efficace pour quantifier l’amplification consiste à utiliser en plus des deux amorces ADN un troisième ADN, appelé « sonde », qui est semblable à une amorce, et qui s’appariera sur une séquence choisie à l’intérieur du fragment à amplifier. Cependant, suite à une modification de ses extrémités, cette sonde ne pourra pas être utilisée comme amorce, et à chaque synthèse du brin d’ADN sur lequel cette sonde est appariée, elle sera bousculée, dégradée et décrochée de l’ADN par la polymérase. Lors de cette « expulsion », un signal fluorescent sera activé, et émettra une quantité bien définie de lumière, qui sera enregistrée par l’appareil. La figure suivante résume cette stratégie.
– Etape 1 : ADN double brin à amplifier ;
– Etape 2 : Appariement (après chauffage) de l’amorce et de la sonde, dont l’émission de lumière par la première base modifiée (C dans cet exemple) est bloquée par la présence d’un inhibiteur indiqué en lettre grasse (T ici) ;
– Etape 3 : La Polymérase en action décroche la sonde qui est coupée en morceaux, permettant l’éloignement de l’inhibiteur de l’émetteur de lumière, qui produit alors son signal.

Interprétation des résultats
La figure suivante est un résultat caractéristique de qRT-PCR. L’axe horizontal représente le nombre de cycles (ici, jusqu’à 45). L’axe vertical (ΔRn) représente la quantité de lumière émise lors de l’amplification des échantillons de départ. Le trait vert horizontal est

utilisé comme référence afin de déterminer après combien de cycles l’échantillon franchit ce seuil, appelé « Ct », pour « Cycle threshold », ou en français, seuil de cycle.
Sur cet exemple, un prélèvement ADN a été amplifié après avoir été dilué 4, 16, 64 et 256 fois. Chaque échantillon est en double afin de s’assurer de la reproductibilité des résultats.
- En absence d’ADN à amplifier, aucun signal ne doit apparaître (contrôle négatif).
- Sur le panneau A, après 25 cycles, le signal apparaît au fur et à mesure de la progression de la réaction sous forme d’un trait pour chaque échantillon.
- Sur la panneau B, la réaction a été continuée jusqu’au cycle 45. On observe que les courbes ne sont plus exponentielles, et atteignent toute, plus ou moins tôt, un même plateau. Ceci est dû à l’épuisement des réactifs nécessaires à l’amplification (nucléotides, polymérase, sondes…). Afin de quantifier les différents échantillons, on s’intéresse au nombre de cycles nécessaires pour franchir le Ct (trait vert).
L’échantillon le moins dilué (dilué 4x) traverse le Ct après 20.6 cycles. Le dilué 16x, après 22.5 cycles, soit 1.9 cycles de plus. Ceci correspond approximativement à une différence de concentration de 21.9 = 3.7, proche des 4x attendus. Le dilué 64x a un Ct de 24.5, soit 2 cycles de plus que le dilué 16x. On obtient donc une concentration plus faible de 22 = 4 fois, exactement comme attendu.
On comprend bien sur cet exemple que plus le passage du Ct est petit, plus l’échantillon de départ est concentré
Dans le cas qui nous intéresse ici, le « test COVID-19 par PCR », on réalise immédiatement que si le résultat est négatif, il n’y a aucune ambiguïté : la personne testée n’est pas porteuse du virus, à condition bien sûr que:
1- le prélèvement ait été correctement effectué,
2- l’extraction du matériel génétique de ce prélèvement ait été correctement effectué.
On peut a priori exclure une erreur de manipulation lors de la qRT-PCR, puisque toute série d’analyses doit être accompagnée d’une part de ce que l’on appelle un contrôle positif, c’est à dire du matériel génétique viral à concentration connue qui doit donner un signal, et d’autre part d’un contrôle négatif, dépourvu de tout matériel génétique ciblé par les amorces, et qui donc ne doit donner aucun signal.
Envisageons maintenant que le résultat soit positif. Si les contrôles décrits plus haut indiquent que les réactions ont été correctement effectuées, alors la personne est déclarée « cas COVID », sous- entendu qu’elle est touchée par la COVID-19.
Cependant, le test PCR, bien qu’il soit un outil très puissant, n’a jamais permis de déterminer si une personne est malade ou non. La seule conclusion que l’on puisse tirer d’un test PCR positif est que dans le prélèvement se trouvait au moins un fragment d’ARN viral capable d’être reconnu par les amorces utilisées.
Ce fragment peut être un reste d’acide nucléique provenant d’un virus détruit part le système immunitaire du porteur. Ou il peut provenir de virus présents chez la personne testés, mais trop peu nombreux pour pouvoir déclencher la maladie.
Malheureusement, les laboratoires d’analyse n’indiquent pas le Ct auquel le signal est apparu lors du test. Un Ct de 20 n’aura évidemment pas la même signification qu’un hypothétique Ct de 50, puisque le virus sera dans le second cas 2(50-20), soit 1.073.741.824 de fois moins abondant que dans le premier cas (oui, un milliard de fois moins abondant !).
De plus, des travaux en laboratoire de recherche ont montré que les « charges virales » (i.e. le nombre de virus) de personnes ayant des Ct supérieur à 34 n’étaient généralement pas suffisantes pour entraîner des infections (3), bien que ces personnes soient déclarées aussi positives que celles ayant des charges virales des milliers de fois supérieures…
Conclusion
Nous avons présenté le principe et la puissance de l’analyse par qRT-PCR. Cet outil reste incontestablement le plus sûr et le plus précis pour mettre en évidence la présence d’un ARN viral SARS-CoV-2 (ou autre virus, avec des amorces adaptées) dans un échantillon. Cependant, nous avons vu qu’être « cas positif » à ce test ne signifie pas que l’on est malade de la COVID-19. Un résultat positif indique effectivement que la personne est au moins porteuse de quelques fragments d’ARN viraux, qui ont été amplifiés, d’autant plus que le nombre de cycles utilisé aura été très élevé (supérieur à 40).
On pourrait idéalement souhaiter voir mentionner sur les résultats de test le nombre de cycles utilisés, et surtout le Ct auquel le signal est apparu. Il est cependant techniquement difficile d’affirmer qu’au delà d’un Ct bien précis, il n’y a aucun risque d’infection. Cela tient au fait que chaque laboratoire, avec un même échantillon, pourra avoir des valeurs de Ct plus ou moins variables. La biologie moléculaire, qui semble une science exacte, est en fait très sensible à de toutes petites variations. Les systèmes PCR peuvent être différents d’un labo à l’autre, les échantillons préparés un peu différemment, etc…
Même l’utilisation d’un standard d’ARN viral de référence dont le Ct théorique est connu ne permettrait pas d’étalonner les labos entre eux, puisque des différences dans le traitement des écouvillons ne seraient pas pris en compte.
Cependant, il semble raisonnable de penser qu’au delà de 35 cycles, la contamination n’est pas biologiquement significative. Pourquoi ne pas concevoir une représentation visuelle des résultats, par exemple une barre colorée du vert au rouge selon les Ct, indiquant aux personnes où se trouve leur niveau réel de risque de contamination?
Par exemple :

Il semble cependant que cela ne soit pas envisagé.
Pourtant, bien des personnes « cas COVID » seraient rassurées si elles avaient accès à leur Ct et si celui-ci les plaçait « dans le vert ».
Laissons à chacun la liberté de s’interroger sur les raisons pour lesquelles une telle présentation n’existe pas aujourd’hui, alors que pour toute analyse de sang classique, les résultats sont systématiquement positionnés entre les valeurs de référence, afin de permettre à la personne testée de positionner son résultat d’analyse par rapport aux limites « acceptables ».
Pour terminer, et bien que la positivité d’un test ne signifie en rien que la personne soit a priori malade, il faut cependant mentionner un intérêt réel de ces tests. Hormis les périodes où même les personnes qui n’auraient pas envisagé de se faire tester le font quand même (vacances de Noël…), seules les personnes inquiètes, à tort ou à raison, vont se faire tester. Sur la masse des tests effectués quotidiennement, on a statistiquement la même proportion de positifs « non significatifs ».
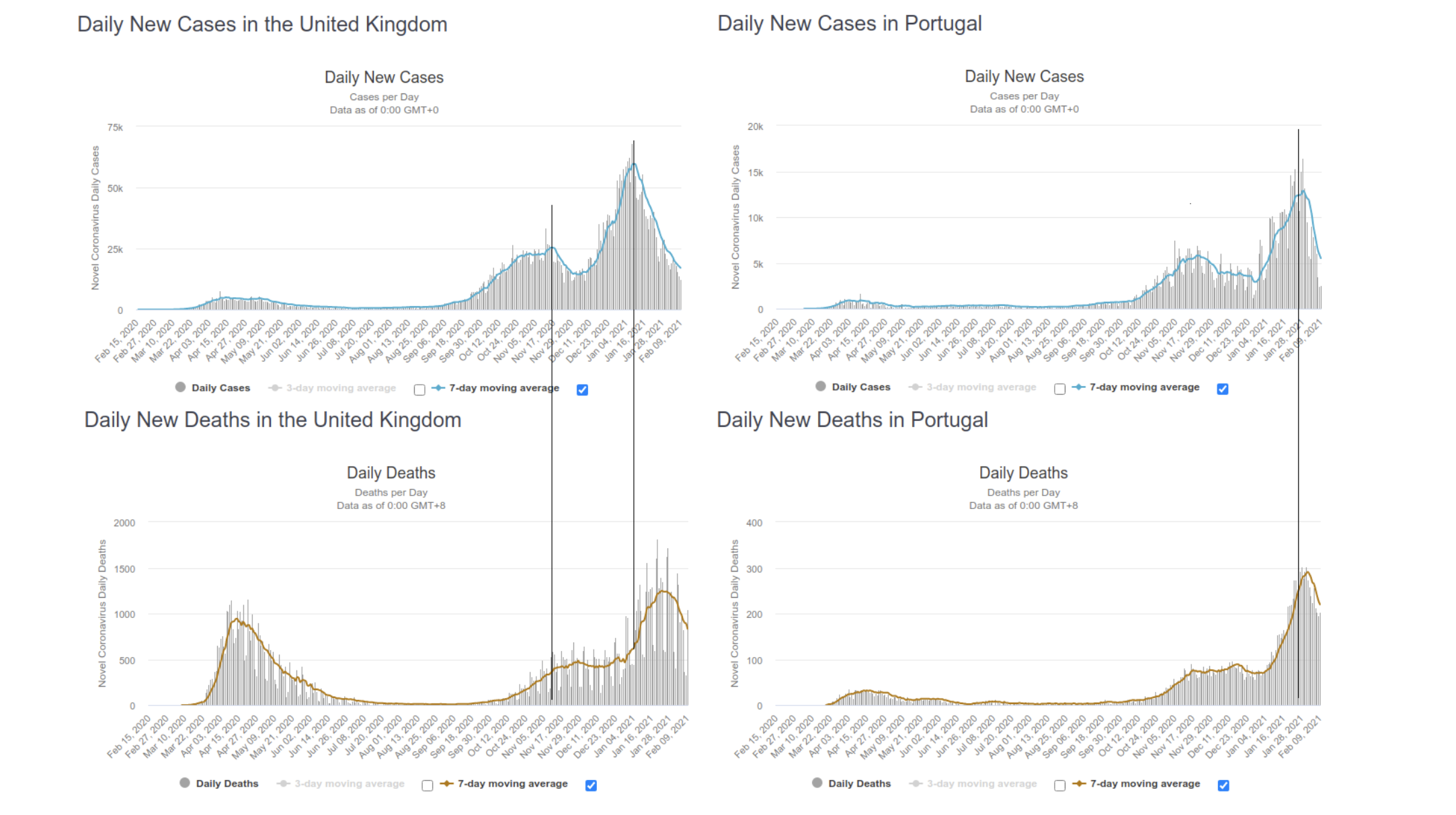
Etant donné que les passages en réanimation consécutifs aux infections par le SARS-CoV-2 n’apparaissent pas avant une semaine environ, et les décès pas avant une dizaine de jours, le suivi de l’évolution du taux de positivité dans la population testée donne une idée de la situation à venir.
Ceci est illustré sur la figure ci-dessous, où des lignes verticales passent sur les sommets des courbes du nombre de cas positifs pour différents pays, et descendent sur les courbes des décès de ces mêmes pays (les dates étant alignées).
On observe que dans la plupart des cas, il existe bien un délai d’une dizaine de jours environ entre le pic de cas positifs et le pic des décès.
Cette observation est d’autant plus solide que bien que chaque pays ait sa façon propre de gérer ses tests, cette observation reste vraie.
Dr Philippe Pognonec
Avril 2021

Notes et sources
(*) https://www.aimsib.org/2020/08/30/covid-le-pcr-nasal-peut-il-mentir/
(**) Philippe Pognonec, Ph.D., Directeur de Recherche CNRS, unités Transporteurs en Imagerie et Radiothérapie en Oncologie, CEA Faculté de Médecine, Université de Nice, 28 Avenue de Valombrose 06107 Nice Cedex 2, France
(1) Saiki, R.; Scharf, S.; Faloona, F.; Mullis, K.; Horn, G.; Erlich, H.; Arnheim, N. Enzymatic Amplification of Beta-Globin Genomic Sequences and Restriction Site Analysis for Diagnosis of Sickle Cell Anemia. Science 1985, 230 (4732), 1350–1354. https://doi.org/10.1126/science.2999980.
(2) Genomes, 2nd ed.; Brown, T. A., Ed.; Wiley-Liss: New York, 2002.
(3) La Scola, B.; Le Bideau, M.; Andreani, J.; Hoang, V. T.; Grimaldier, C.; Colson, P.; Gautret, P.;
Raoult, D. Viral RNA Load as Determined by Cell Culture as a Management Tool for Discharge of SARS-CoV-2 Patients from Infectious Disease Wards. Eur. J. Clin. Microbiol. Infect. Dis. Off. Publ. Eur. Soc. Clin. Microbiol. 2020, 39 (6), 1059–1061. https://doi.org/10.1007/s10096-020- 03913-9.












J’ai entendu dire que certains tests amplifiaient jusqu’à 3 séquences du génome du virus. Ces tests devraient donc être plus spécifiques que ceux qui n’amplifient qu’une seule séquence. La valeur Ct est alors obtenue pour chacune des séquences. Pour avoir un test positif, il faudrait être positif pour les 3 séquences, mais j’ai entendu dire que (ce n’était pas toujours le cas) une des 3 séquences testée positive suffisait pour déclarer le test positif. Si c’est le cas, un test sur 3 séquences de cette façon devient moins spécifique qu’un test sur séquence unique. Comment gonfler le taux de positivité…
Cher Joss, les 3 séquences ciblent différentes régions de la séquence d’ARN du virus. Une mutation peut affecter l’efficacité d’amplification par PCR. Ainsi, utiliser 3 régions différentes permet de detecter l’ARN du SarsCov2, quand bien même il s’agirait d’une version mutée. Reste que la technique de la PCR est extrêmement spécifique en soit : « La seule conclusion que l’on puisse tirer d’un test PCR positif est que dans le prélèvement se trouvait au moins un fragment d’ARN viral capable d’être reconnu par les amorces utilisées. » C’est déjà une bonne information quand on veut maitriser la propagation de l’épidémie. Je rajouterai que sachant que le virus migre au sein du corps au cours du temps, l’interprétation du CT d’un prélèvement nasal à un moment t est délicat, pour ne pas dire hasardeux. Surtout si c’est pour décider de l’isolement ou non de la personne infectée.. A quoi bon l’indiquer?
En dehors de mon domaine mais terriblement précis et clair, bravo.
Est-ce la répétition du test (nouveau prélèvement) après chaque résultat positif pourrait réduire le nombre de faux positifs ?
Pierre Biron
C’est bien ça le problème, comme expliqué par Cathy, lorsque une personne est notée positive, même si le tests suivant est négatif elle reste positive pour les statistiques!
La répétition des tests fausse les statistiques., les cas positifs étant souvent retestés.
Le site https://www.cascoronavirus.fr/test-depistage/france qui se base sur source Santé publique indique à la date du 21 avril 2021 sur 73.535.714 tests réalisés (plus que la population française) un taux de positifs de 7,1%. Tests négatifs 68 289 157 (92.9 %)
En reprenant un de mes commentaires du 21 septembre 2020 à 7h10 (article Descente d’une « Brigade Sanitaire » dans une école maternelle) le taux de positifs n’était pas de la moitié !
Les données des tests de dépistage du Coronavirus COVID-19 sont datées du 16 septembre 2020 par Santé publique.
8 988 790 Tests réalisés
299 983 (3.3 %) Tests positifs
8 688 807 (96.7 %) Tests négatifs
Est-ce l’introduction des tests salivaires, et antigéniques moins précis qui expliquerait cet écart ?
1500 personnes testées positives aux USA ont été examinées et prélevées: chez aucune on n’a trouvé de virus covid. Par contre, de la grippe A ou B, comme tous les ans.
Le test covid est donc bien frauduleux, et c’est pourtant sur lui que reposent toutes les mesures qui nous tyrannisent.
L’auteur de l’article est bien gentil, quand il fixe la barre significative à 35 cycles: à ce niveau, la fiabilité est de 3%…
http://www.brujitafr.fr/2021/04/usa-les-laboratoires-americains-ne-trouvent-aucun-covid-19-dans-plus-de-1-500-tests-positifs.html?utm_source=_ob_email&utm_medium=_ob_notification&utm_campaign=_ob_pushmail
Je rappelle qu’un immense procès international par l’avocat Reiner Fuellmich contre le promoteur allemand du test PCR (Chritian Drosten) est sur le point d’être mis en place. Il faudra suivre l’affaire de près, ses conséquences sont incalculables, et le scandale international à suivre gigantesque.
Tu imagines à quel point tout le monde l’attend?
Laz bataille des cycles ne fait que se poursuivre, je te rappelle qu’on revient de 50 Ct. Emma Kahn souhaiterait un bridage à 28….
@Vincent
Une vraie info, sans rire:
Le PDG de YouTube, Susan Wojcicki, a reçu le prix « Free Expression » du Freedom Forum Institute lors d’une cérémonie virtuelle parrainée par YouTube, plate-forme de vidéos en ligne appartenant à Google.
Wojcicki, dans une interview lors de la cérémonie en ligne, a souligné l’importance de la liberté d’expression et le rôle que joue YouTube dans sa protection.
(Non, vous ne rêvez pas…)
https://urlz.fr/furU
Ici, en fin de vidéo, révélé par projet veritas, écoutez le responsable de CNN se vanter d’avoir utilisé à mort la peur pour augmenter l’audience (à 12’26 »): plus cynique, tu meurs…
https://infovf.com/video/crise-sanitaire-faut-contrer-propagande-mediatique–9059.html
Enfin pour vous remonter le moral et respirer un peu d’air pur au milieu de la pourriture ambiante, écoutez Christian Perronne:
https://www.francesoir.fr/societe-sante/youtube-censure-perronne-entretien
d’après les plus récentes publications, au-dessus de Ct 28-30, il n’y a pas de virus viable (cultivable)
Un scandale gigantesque ? Potentiellement gigantesque mais attention quand même, il y eut dans le passé, en médecine et pas qu’en médecine, d’énormes scandales potentiels qui ont été étouffés et justement parce qu’ils étaient gigantesques. Je pourrais en donner des exemples. J’en avais d’ailleurs présenté plusieurs ici même dans des articles Aimsib mais ils n’ont pas forcément retenu l’attention de beaucoup en raison même de la distance historique ou de la difficulté technique. Par exemples :
Le vaccin antivariolique à virus vivant ayant conservé la capacité de se répliquer aggravait la variole chez des non immunisés et la provoquait chez des immunisés (par une ancienne vaccination ou une ancienne variole) quand la vaccination était réalisée pendant l’incubation ou quelques jours avant le contage. Cela avait été mis sur la table dès 1870 mais écrasé jusqu’à ce que les expérimentations sur des singes réalisées en 2005-2008 ouvrent enfin les yeux et éclairent enfin les mystères observées au cours de la campagne d’éradication (et auparavant). Voir mes articles aimsib de déc. 2019, mai et sept. 2020. Aujourd’hui « ils » le savent (et je sais qu’ils le savent, secret de couloirs de congrès … ) mais les conséquences rétrospectives sont si énormes que cela ne sera jamais reconnu. .
2- Il y a les tests PCR dont vous parlez mais il y a aussi d’autres tests, les tests statistiques utilisés n’importe comment non seulement par les auteurs d’études épidémiologiques qui auraient mal appris leurs leçons mais par la discipline elle même, l’épidémiologie et à l’internationale. Le clou de la soirée reste l’utilisation du test dit cas-témoins pour tester sur des délais c’est à dire quand le facteur d’exposition est de la forme « la maladie apparait dans l’année qui suit une vaccination » (par exemple). C’est d’une aberration totale et cela conduit à neutraliser des signaux existants ou à en faire apparaitre qui n’existent pas. J’avais aussi donné toutes les explications à ce sujet dans des articles aimsib. Les conséquences peuvent être énormes comme je l’avais aussi montré. Malheureusement, la petite difficulté technique inerrante à cela rebute beaucoup de lecteurs et commentateurs. C’est plus que dommageable.
Des fautes de cette nature peuvent paraître mineures par rapport à ce que nous constatons avec cette pandémie. On a grand tort de le voir ainsi car ces erreurs incroyables s’appliquent de multiples façons et ont joué un rôle déterminant dans les conclusions aujourd’hui acceptées de l’absence de lien entre vaccination hépatite B et SEP alors qu’une analyse plus sérieuse des données publiées montre le contraire.
Est-ce que vous vous rendez compte des conséquences quand on constate que les 72 tests de la publication américaine Langer-Gould sur le lien entre vaccinations et démyélinisation sont tous non valables pour cette raison (tous en cas-témoins sur des délais). Qu’il en va de même pour plus d’une centaine de tests dans les publications Mikaeloff-Tardieu sur le même thème et que les autres tests de ces publications qui ne sont pas frappées par cela ne sont pas valables non plus pour d’autres raisons. Autrement dit, il ne reste rien des études faites dans ces ces publications en dehors des données rapportées.
Bonjour , forcément , beaucoup de gens se sont posé la question du pourquoi en mai 2020 , il n’y avait eu que 72 morts de la grippe . Puis,fin octobre , une nouvelle annonce déclare 3800 morts (bien sur , après déterrage et autopsie,cela va de soit …chiffres pour mettre fin à la polémique,surtout) . Puis , on a su Le 18 septembre2020 que la HAS a rendu un avis favorable à l’utilisation de
ces tests pcr uniquement chez les personnes présentant des symptômes(source : le monde) . ah bon ? donc , problème avec les tests de masse ?…eh bien peut être …puisque plusieurs fois , les autorités officielles comme le CDC , oms nous font comprendre la méme chose.
Puis , de la Haute autorité de santé , un nouveau doc. Et question :Pourquoi faire aux gens hospitalisés du multitest pour distinguer les virus covid et grippe si un seul test suffit et fiable ???? … tiens donc , on ne le fait pas dans la rue de plus ! Y a t il qque chose que je n’ai pas compris ?
https://www.has-sante.fr/jcms/p_3213581/fr/distinguer-la-grippe-de-la-covid-19-dans-quelles-situations-et-avec-quels-tests
Et de méme , un labo Roche qui a voulu distinguer le sarscov2 de la grippe .C’est bien écrit : DISTINGUER;
https://www.sudouest.fr/2020/09/04/coronavirus-le-laboratoire-roche-obtient-un-feu-vert-pour-son-test-qui-distingue-grippe-et-covid-19-7806457-10997.php?nic
Cela corrobore , certes votre document concernant les 1500 personnes testées positives à l’université …
Beaucoup de personnes disent que c’est impossible d’avoir des test positifs covid pour de la grippe ( même si , entre sarscov2 et virus grippal , il y a un certain pourcentage identique entre génome).
Il existe aussi différents tests pcr , peut etre que certains fonctionnent mieux que d’autres . Bien à Vous.
Bonjour merci pour cet article intéressant; Vous allez peut être pouvoir m’expliquer quelque chose. J’ai eu le covid en octobre 2020 . Test PCR positif, c’était évident.
Fin février 2021, lors d’un séjour hospitalier , test PCR obligatoire. Le médecin vient m’indiquer que je suis positive. Je ne comprends pas comment j’aurai pu être contaminée. je le dis aux médecins. second test PCR , d’après eux plus poussé? Je ne comprends pas ce que cela signifie. Le test revient négatif. Je demande comment le premier a pu revenir positif; Ils m’indiquent, soit que j’avais encore des reliquats du virus (si je comprends bien il me restait de l’arn du virus dans le nez) ou alors j’étais un « faux positif » donc si j’ai bien suivi, le ct était sans doute supérieur à 40. A l’annonce du premier test positif, j’ai été considérée comme un paria . J’ai reçu un appel de la CPAM qui m’a indiqué qu’étant signalée comme positive, je devais rester confinée etc; Quand je leur ai parlé du second test invalidant le premier, la personne m’a dit qu’elle ne pouvait pas « annuler » ma fiche et que je serai comptée comme positive… Pourquoi ne pas dire le nombre de cycle à ce moment là? Est-ce que le numéro de ct qui apparait peut prédire une éventuelle contagiosité? Suis je plus contagieuse à 20 ou 25 ct ?? La première fois, malgré une positivité flagrante , j’ai été assez malade mais mes poumons n’ont pas été atteints, aucun membre de ma famille n’a été atteint. (Dés l’apparition de la fièvre je me suis isolée. ) . merci pour votre réponse. (qu’en est il des autres tests antigéniques, autotests et test salivaire? )
Cathy, aviez-vous eu à chaque test le nom du kit réactif et le Ct?
Sans cela on ne peut rien dire!
Les Ct supérieurs à 28-30 sont sans doute des faux positifs : morceaux d’ARN dégradés excrétés bien après l’infection
Bonjour Emma, comme j’étais en centre hospitalier, je n’ai pas eu la copie des tests. J’ai eu un compte rendu sur lequel il est noté premier prélèvement ininterprétable. Le second est noté négatif. Pourtant j’ai reçu deux enveloppes avec 4 pages d’informations et un appel de la CPAM me demandant de rester confinée et d’éviter tout contact avec ma famille. Je leu ai demandé de supprimer ma fiche puisque j’étais en fait négative. Il m’a été indiqué que ce n’était pas possible.
Vue la complexité de ce qui vient d’être , je ne suis pas étonné du « bordel » qui « règne » dans la tête des politiques de tous bords, et dans celles de nos « dirigeants » déboussolés !!!….. Aï-ta péa- péa !!!…..
Vous oubliez tous le détail qui tue, c’est qu’avant toute chose il faut une amorce valide et dans le cas du Sars Cov 2 c’est loin d’être le cas. La validité d’un génome fait par consensus est aléatoire, le Sars Cov 2 n’est toujours pas isolé et purifié .De qu’elle soupe les protéines ont étés extraites?? Dans le cas du VIH par exemple la P 24 « soit disant spécifique au VIH » à été signalé dans de nombreux tissus comme la P 41 d’ailleurs. La soupe dans laquelle Montagnier à péché ses poissons était loin d’être limpide. Les tests PCR n’ont jamais été validé cela reste un outil de laboratoire et spéculer dessus revient à accepter de fait une méthode que même son créateur à dénoncé l’usage qui en est fait. Je vous ramène au travaux du Group de Perth qui explique très bien les choses https://www.youtube.com/watch?v=LB2JyBnlE7w Tout cela n’est que de la mauvaise science, une escroquerie.
Bonjour à tous. « le Sars Cov 2 n’est toujours pas isolé et purifié .De qu’elle soupe les protéines ont étés extraites?? » Je me pose la meme question. D ‘autant que le 4 iéme postulat de Kock n est pas respecté. Mais quand meme, ils ont bien isolé quelque chose ? un corona qui passait par là ? Si les séquençage ont lieu, notamment à Marseille c’est bien que quelque chose a été isolé.
https://youtu.be/3g1NKqhK8lg.
Francis Lalanne : « Ils sont beaux nos sourires »
Merci à l’auteur de cet article pour ces explications et surtout sa conclusion.
Une question cependant, comment plusieurs tests PCR peuvent ils être négatifs sur un personne malade du Covid et plutôt fortement alors que l’ analyse d’une prise de sang à la fin (soigné seulement par le Parcétamol et attendre le SAMU le cas échéant… ) a montré qu’elle avait finalement bien été « Covidée » – c’est le cas de le dire , vidée de ses forces – celle ci ayant montré qu’elle avait les anticorps et qu’en outre, un scanner a montré « un voile au poumon » , caractéristique de cette maladie ?
Bonjour,
Le test PCR est positif en présence du SARS-CoV-2, virus pouvant déclencher la Covid-19 chez la personne contaminée.
Au cours de la maladie, si maladie il y a, le virus disparaît après une à deux semaines, et seuls les conséquences de l’infection (« orage de cytokines », par exemple) maintiennent éventuellement les malades à l’hôpital.
Donc, un malade en réa plusieurs semaines après l’infection sera négatif pour le virus. Par contre, son système immunitaire ayant répondu à l’infection, sa réponse à un test antigénique, qui détecte les anticorps produits par ses cellules sanguines contre le virus lors de l’infection, sera positive.
Ceci est tout à fait dans l’ordre des choses.
Il existe une vidéo de l’excellent statisticien Pierre de la chaîne YouTube Décoder l’Eco, consacrée à la folie des tests RT-PCR (La dictature des tests – vidéo 18 min – 22 février 2021) :
https://youtu.be/WNPpqoe2JOo
« Pourquoi ne pas concevoir une représentation visuelle des résultats, par exemple une barre colorée du vert au rouge selon les Ct, indiquant aux personnes où se trouve leur niveau réel de risque de contamination? »
L’idée colorée me paraît équivoque, car elle suppose qu’au delà d’un certain CT mettons ⩾ à 30 ou 33, la personne serait peut-être (?) contaminante, alors que le test PCR n’a détecté que des débris d’une ancienne infection qui ne peuvent être contaminants. Il n’y a que les virus vivants qui peuvent se transmettre. On retrouve la même équivoque dans les documents des autorités de santé, et dans les documents de la Société Française de Microbiologie (SFM) qui, quel que soit le CT parle « d’excrétion virale », même si elle y ajoute des qualificatifs « modérée voire très faible » !
Entre excréter des virus ou des débris ce n’est pas la même chose ! et « mal nommer les choses c’est ajouter au malheur du monde » comme disait Camus.
Les seules données objectives ne peuvent qu’être des données quantitatives, et bien que la SFM ait été questionnée sur le sujet par la DGS en septembre 2020, les données restent seulement « qualitatives ». Cette Société n’encourage pas les biologistes à communiquer des infos sur leur matériel, et les CT utilisés :
Avis du 25 septembre 2020 de la Société Française de Microbiologie (SFM) relatif à l’interprétation de la valeur de Ct (estimation de la charge virale) obtenue en cas de RT-PCR SARS-CoV-2 positive sur les prélèvements cliniques réalisés à des fins diagnostiques ou de dépistage Version 1 _ 25/09/202
(……)
5. Méthodologie et réponses du groupe d’expert
(…) En revanche, en raison de son caractère seulement semi-quantitatif et des variations inter-techniques, le groupe d’experts ne pense pas qu’il soit recommandé de faire figurer systématiquement cette valeur sur les comptes-rendus de résultats. Le biologiste médical reste à même de décider si cette valeur doit être diffusée aux prescripteurs en fonction des besoins et expertises. Le groupe d’experts rappelle également que pour certaines techniques de RT-PCR, le rendu est uniquement qualitatif ou exprimé en valeurs numériques non corrélables aux valeurs de Ct usuelles (tests non RT-PCR, tests multiplex …)
(…)
Le biologiste médical peut donc, après évaluation locale ou à l’aide de l’abaque des valeurs de Ct obtenue comparativement à la technique du CNR IP4 (cf. annexe), établir la catégorie d’excrétion virale. Il est recommandé de suivre pour les trousses commerciales les règles d’interprétation données par le fournisseur si elles sont disponibles. En plus de ces règles, et selon le nombre de cibles virales positives et la valeur du Ct de la cible la plus sensible, le biologiste peut rendre un résultat qualitatif comme suit :
-Si toutes cibles détectées (1/1, 2/2 ou 3/3) avec Ct de la cible la plus sensible ≤ 33,rendre «Positif »
-Si 2 cibles sur 3 avec Ct de la cible la plus sensible ≤ 33, rendre «Positif »
-Si 2 cibles sur 3 avec Ct de la cible la plus sensible > 33, rendre «Positif faible»
-Si toutes cibles détectées (1/1, 2/2 ou 3/3) avec Ct > 33, rendre «Positif faible»
-Si uniquement 1 cible détectée sur 1 avec Ct > 33, rendre « Positif faible»
-Si uniquement 1 cible détectée sur 2 ou 3 avec Ct 33, la présence d’ARN viral détecté est compatible avec une excrétion virale modérée voire très faible
(…)
Ainsi, la valeur de Ct de la cible la plus sensible de la technique utilisée (comparée à la technique de référence IP4 peut être interprétée concernant l’importance de l’excrétion virale comme suit (cf. algorithme infra) :
-Si la valeur de Ct est ≤ 33, la présence d’ARN viral détecté est compatible avec une excrétion virale significative
-Si la valeur de Ct est > 33, la présence d’ARN viral détecté est compatible avec une excrétion virale modérée voire très faible
(…)
https://www.sfm-microbiologie.org/wp-content/uploads/2020/09/Avis-SFM-valeur-Ct-excre%CC%81tion-virale-_-Version-Finale-25092020.pdf
https://www.sfm-microbiologie.org/covid-19-fiches-et-documents-sfm/
donc vous l’aurez compris, quel que soit la valeur du CT, si votre test est positif vous êtes supposé contaminant, comptabilisé « Covidé » et prié de vous plier à une quarantaine, même si vous êtes complétement asymptomatique.
Le pire est que toute cette histoire de pandémie est construite là-dessus !
Il y a plus énigmatique ! Il y a des pays dans le monde, où il n’y a que très peu de morts du Covid. La Mongolie par exemple n’avait que 2 morts jusqu’à fin février 2021. Puis la campagne de vaccination a débuté. On en est à plus de 80 morts.
https://vk.com/photo444549918_457239864?rev=1
Cette histoire de vaccination à ARNm fait peur, car comme le Dr Morgan le révèle, il est possible de programmer une cellule et la diriger pour cibler n’importe quelle partie du corps, y compris le cerveau qui peut alors également être reprogrammé et contrôlé à partir d’une force extérieure. Des nanobots miniatures de la taille de particules de poussière peuvent être programmés pour attaquer n’importe quelle partie du corps pour délivrer une charge utile ou un virus directement dans la circulation sanguine, les organes, le cerveau, les yeux, etc. Ils peuvent également rester en sommeil dans n’importe quelle partie du corps vers laquelle ils ont été dirigés et peuvent y rester sans être détectés jusqu’à ce que le signal électronique approprié soit délivré pour les réactiver. Le 13 juin 2018, le Dr Charles Morgan, a donné une conférence devant les étudiants de l’Académie militaire de West Point (USMA). Il a parlé de la capacité de modifier l’ADN à des fins de contrôle de l’esprit. N’est-il donc pas dangereux de se faire vacciner alors qu’il existe aujourd’hui plusieurs traitements ?
https://www.youtube.com/watch?v=cTtIPBPSv0U
C’est fou le nombre de fake news sur le coronavirus ! Dernier en date en Inde :
https://lesmoutonsenrages.fr/wp-content/uploads/2021/04/nypost.png
La réalité :
https://lesmoutonsenrages.fr/wp-content/uploads/2021/04/tv5monde.png
Toute cette histoire de pandémie sans fin repose sur les tests PCR et dérivés plus récents, ainsi que l’indique d’ailleurs l’avocat Reiner Fuellmich, l’imposture Drosten sera l’angle d’attaque dans les recours juridiques.
Le gouvernement s’apprête à tester massivement dans les écoles (« avec un objectif de 600 000 d’ici la mi-mai), collèges, lycées… (« et d’ici juin, nous monterons en puissance avec potentiellement un million de tests hebdomadaires » dixit JM Blanquer) sur de jeunes enfants, ados dont nous pouvons supposer qu’ils ne sont pas malades s’ils se rendent dans leur établissement scolaire.
Or, une étude chinoise publiée en novembre 2020* portant sur 10 millions de personnes à Wuhan révèle que les personnes positives asymptomatiques au Covid ne sont pas contagieuses, seuls les malades pourraient transmettre le virus. Silence dans les médias, pourquoi ?
* Post-lockdown SARS-CoV-2 nucleic acid screening in nearly ten million residents of Wuhan, China
https://www.nature.com/articles/s41467-020-19802-w
source : http://www.profession-gendarme.com/porteurs-asymptomatiques/
Il faut savoir que suivant le dernier protocole dans les écoles qui doit être le 25 ou 26ème depuis le mois de septembre, un seul cas testé positif entrainera la fermeture de la classe ! dans la période avant Pâques il en fallait 3 !
Merci, Docteur pour ce topo définitif sur ce sujet important et pas commode du tout.
Cependant, d’accord avec Njama, le vieux soudard social que je demeure est totalement opposé à cette mode des ‘’CODES’’ COULEUR.
Elle infantilise (le rêve !) le consommateur (défendu par mes 3 filles), méprise les daltoniens, confine les chiffres chez les sachants prétendus, et cache les concentrations les plus criminelles [l’aluminium hyperneurotoxique dans l’eau potable, le cadmium et le cobalt cancérogènes ainsi que les immunotoxiques ( »perturbateurs endocriniens ») dans les peintures, etc]. Dans l’alimentation, elle prépare le désétiquetage des concentrations de SATURÉS (lentement cancérogènes) à l’initiative du lobby du gras colonial, lobby qui a déjà fait supprimer par l’U€ en 2020 les teneurs en di- et tri-insaturés (teneurs indispensables à leur équilibrage par le consommateur autour du rapport 4) et de SUCRE (lentement tueur par le foie) à l’initiative du lobby du sucre, lobby ligué avec le précédent pour calomnier l’indispensable cholestérol au service des pharmas].
Elle vise surtout à camoufler les DÉRIVES SUBREPTICES dans les normes (qui, comme chacun affecte de l’ignorer, ne recouvrent que des rapports de force sans études justificatives dignes de ce nom). À quand un code des féminicides (par villes ou opinions politiques) ?
La longueur des amorces ainsi que la standardisation de ces dites amorces en fonction des fabricants de tests ne peuvent-ils pas influer ?
Je me souvient d’une équipe de médecins indépendants espagnols il y a quelques mois qui avaient vu qu’outre le nombre de cycles, la faible spécificité des amorces faisait que les séquences analysées se retrouvaient en fait dans plusieurs dizaines d’autres organismes/virus, et même dans des cellules du système humain en faisant un matching avec la banque de données BLAST…
Pour garder la bonne humeur, le joyeux virus #HK #Kaddour #Saltimbanks DANSER ENCORE poursuit sa route à travers l’Europe, ici un nouveau « variant » catalan
https://www.youtube.com/watch?v=vaeayw-iwMM&t=2s
Seules de très rares personnes portent un masque à Barcelone ! La situation devient de + en + ubuesque, le port obligatoire de cette « chiffe » en France, et simultanément liberté dans d’autres pays .
Pour recoller au sujet de l’article :
The WHO Confirms that the Covid-19 PCR Test is Flawed: Estimates of “Positive Cases” are Meaningless. The Lockdown Has No Scientific Basis
(L’OMS confirme que le test Covid-19 PCR est défectueux: les estimations des «cas positifs» sont dénuées de sens. Le verrouillage n’a aucune base scientifique
By Prof Michel Chossudovsky
Global Research, April 23, 2021
https://www.globalresearch.ca/nucleic-acid-testing-technologies-use-polymerase-chain-reaction-pcr-detection-sars-cov-2/5739959
Tous les articles de Global Research peuvent être lus en 27 langues en activant le menu déroulant «Traduire le site Web» sur le bandeau supérieur de notre page d’accueil (version bureau).
Et donc en activant la traduction en français vous pourrez lire que :
Le test de réaction en chaîne par polymérase de transcription inverse en temps réel (rRT-PCR) a été adopté par l’OMS le 23 janvier 2020 comme moyen de détecter le virus SARS-COV-2, suivant les recommandations d’un groupe de recherche en virologie (basé à l’ Université de la Charité Hospital, Berlin), soutenu par la Fondation Bill et Melinda Gates. (Pour plus de détails, voir l’ étude Drosten )
Exactement un an plus tard, le 20 janvier 2021, l’OMS se rétracte. Ils ne disent pas «Nous avons fait une erreur». La rétraction est soigneusement formulée.
Si l’OMS ne nie pas la validité de ses directives trompeuses de janvier 2020, elle recommande néanmoins le « R e-testing» (ce que tout le monde sait être une impossibilité).
…
le reste à découvrir
bonne journée
Oui njama, « Danser encore » la première fois que je l’avais entendue je l’aurais écouter indéfiniment. Les artistes ont compris que plutôt que d’attendre que les salles de spectacles réouvrent à nouveau ils seraient plus utiles à descendre faire le spectacle dans la rue et avec cette chanson ils nous libèrent.
C’est vrai que le virus « danser encore » se répand dans toute l’Europe avec de multiples variants et même avec des passages en français. C’est FORMIDABLE et cela apporte l’ESPOIR. LA VIE est encore là, elle vibre, elle danse …
La contamination va plus vite que prévue ici un nouveau « variant » italien
Danzare ancora, Bologna
https://www.youtube.com/watch?v=Sn-MBJdEc08
Et sur ce site allemand, cette pancarte en français :
« Bonjour la France
Merci pour cette chanson merveilleuse !
On vient de faire notre premier flashmob au cœur de Berlin »
Wieder tanzen gehn! … »Danser encore » deutsch / Berlin 17.04.2021
https://www.youtube.com/watch?v=b13VlKOX9kg
ça réchauffe le coeur !
A regarder les Allemands, les Italiens et d’autres avec cette joie de vivre qui éclate partout je me dis que cette chanson a un secret qui pourrait être un rythme « protéidique » je veux dire qui serait une musique associée, involontairement, à certaines protéines humaines.
On sait depuis longtemps que la musique de Mozart favorise la lactation des vaches. Le physicien Joël Sternheimer a montré que la musique de Mozart contient des séquences qui correspondent à « la musique » des protéines du lait de vache. A chaque accrochage d’un acide aminé il y a une onde très brève de haute fréquence et qui dépend de l’acide aminé. Il y a 4 accrochages par seconde ce qui fait une « musique » non audible sur 20 notes avec 4 notes par seconde. On peut transformer cette musique inaudible en musique audible en dégradant les fréquences mais en conservant leurs rapports. C’est la musique des protéines, les protéodies selon le terme crée par Joël Sternheimer et dont les effets sur la santé humaine, animale et végétale peuvent être très puissants.
Le secret du succès international prodigieux de « danser encore » pourrait être là. Observez la joie des gens sur les places de La Rochelle ou de Berlin par exemples, c’est très étonnant.
La Rochelle : https://www.youtube.com/watch?v=wIuEh-cm6J0
La France a désormais son vaccin qui s’exporte dans toute l’Europe et il s’appelle « Danser Encore ».
Je viens de trouver ça qui est une source d’espoirs :
https://www.sonicmedecine.com/post/la-melodie-du-coronavirus
« Markus Buehler, professeur en ingénierie au Massachussets Intitute of Technology a retranscrit la molécule du Corona Virus, en protéodies (protéine-mélodie). En transposant la structure des protéines en sons, le professeur estime pouvoir mieux étudier et découvrir comment se protéger du virus.
Petit retour en arrière, le pouvoir des protéodies (protéines-mélodies) a été découvert par le physicien Joël Sternheimer. Toute particule a une vibration, une fréquence. Les protéines sont constituées de chaînes de molécules nommées acides aminés qui s’agencent entre elles. A chaque acide aminé d’une protéine correspond une onde. Une molécule est donc une suite de fréquences, une mélodie pour ainsi dire. Lorsque nous transposons ces suites de fréquences à une octave audible, nous obtenons alors la mélodie d’une molécule : une protéodie. Et, fait remarquable, en écoutant une protéodie, l’effet de la molécule se fait ressentir. Cela a conduit à un nouveau concept de biologie ondulatoire, la génodique, qui trouve ses applications dans les domaines agro-alimentaires, énergétiques , environnementaux et médical.
Markus Buehler, professeur en ingénierie au Massachussets Intitute of Technology étudie l’effet des protéodies depuis quelques années. Il a donc entreprit de retranscrire la molécule du Corona Virus en protéodies. En transposant la structure des protéines en sons, le professeur estime pouvoir mieux étudier et découvrir comment se protéger du virus. Pour ce faire, le chercheur américain utilise un logiciel pour convertir les vibrations moléculaires, les structures protéiques, en musique.
«Nous pensons que l’analyse du son et de la musique peut nous aider à mieux comprendre le monde matériel. L’expression artistique n’est, après tout, qu’un modèle du monde en nous et autour de nous», explique le professeur du MIT. Les puissantes capacités de traitement d’analyse du son par le cerveau lui permettent d’identifier des caractéristiques telles que le timbre, la hauteur, le volume, le rythme, la mélodie et l’harmonie. Ces données qui permettent d’avoir une représentation complète de la protéine ne pourraient être étudiées et identifiées visuellement, un microscope de grande puissance ne suffirai pas. Selon Buehler « le son est un moyen si élégant d’accéder aux informations stockées dans une protéine.»
https://vk.com/photo584015149_457250403
Un peu d’humour !
Cela va p’t-être faire bondir Emma Kahn et d’autres virologues, mais je risque…
L’équipe allemande de Samuel Eckert et le Fonds Isolate Truth ont promis une récompense de 1,5 million d’€uros (265.000 dollars) pour tout scientifique capable de fournir des preuves incontestables que le virus SRAS-CoV-2 a été isolé et donc existe. Ils ont également souligné qu’aucun laboratoire dans le monde n’a encore réussi à isoler ce virus corona.
(site en allemand et anglais)
All virologists, not just those pictured, have deceived themselves and the public when they claim the existence of disease-causing viruses such as SARS-CoV-2.Virologists inadvertently kill cells in test tubes, believing that this is proof of the presence and isolation of a virus. Only from fragments of dying cells do virologists mentally construct a gene sequence and pass it off as fact. Therefore, the test procedures do not offer any significance or meaning. Typical structures of dying cells in the electron microscope are passed off as viruses. Such structures could never be detected or recognized in a human being so far!
Our goal
These misguided developments have distanced medicine far from the reality and understanding of true health. We would like to contribute to a comprehensive understanding of disease and health for all people.
We guarantee:
1,5 million € for a virologist who presents scientific proof of the existence of a corona virus, including documented control attempts of all steps taken in the proof.
You’re on!
https://www.samueleckert.net/isolat-truth-fund/
(trad. Deepl) Tous les virologues, et pas seulement ceux qui sont représentés sur la photo, se sont trompés eux-mêmes et ont trompé le public lorsqu’ils ont affirmé l’existence de virus responsables de maladies telles que le SRAS-CoV-2. Ce n’est qu’à partir de fragments de cellules mourantes que les virologues construisent mentalement une séquence génétique et la font passer pour un fait. Les procédures de test n’offrent donc aucune signification ni aucun sens. Au microscope électronique, les structures typiques des cellules mourantes sont présentées comme des virus. De telles structures n’ont jamais pu être détectées ou reconnues chez un être humain jusqu’à présent !
Notre objectif
Ces développements malencontreux ont éloigné la médecine de la réalité et de la compréhension de la véritable santé. Nous souhaitons contribuer à une compréhension globale de la maladie et de la santé pour tous.
Nous offrons
1,5 million € pour un virologue qui présente une preuve scientifique de l’existence d’un virus corona, y compris des tentatives de contrôle documentées de toutes les étapes de la preuve.
C’est parti !
Ma parole mais tu n’as jamais vu Emma en colère? :-)))
euh … J’ai cherché qui était ce Samuel Eckert, je n’ai rein trouvé sur ses compétences, il a une chaîne Youtube qui il est ??? Attention, peut-être encore un faux ou un fantaisiste .
Non, jamais vu, j’préfère pas… mais elle pourrait décrocher la timbale, 1,5 million d’€ tout de même !
et puis en relation avec l’article … le CDC est poursuivi pour fraude massive, il admet qu’il n’y a pas de virus identifiable, c’est le coronacircus cette histoire de PCR
Laboratories in US can’t find Covid-19 in one of 1,500 positive tests
by GreatReject · 11/04/2021
CDC sued for massive fraud: Tests at 7 universities of ALL people examined showed that they did not have Covid, but just Influenza A or B – EU statistics: ‘Corona’ virtually disappeared, even under mortality.
(……) CDC itself admits to having no identifiable virus
Deeply hidden in an official document on Covid-19 [ https://www.fda.gov/media/134922/download ], the CDC ruefully admitted as early as summer 2020 that it does not have a measurable virus: ‘As no quantified (= measured) isolated virus objects of 2019-nCoV are taillable at this time…’ (page 39 of the ‘CDC 2019-Novel Coronavirus (2019-nCoV) Real-Time RT-PCR Diagnostic Panel’ (July 13) In other words, the CDC, as one of THE leading medical authorities in the world, could not, and still cannot, demonstrate a virus.
About the for this purpose scientifically totally debunked, but still shamelessly abused PCR test, the CDC wrote under the heading ‘limitations’: ‘The detection of viral RNA cannot demonstrate the presence of an infectious virus, or that 2019-nCoV is the causative agent of clinical symptoms.’ And in addition: ‘This test cannot exclude other diseases caused by other bacterial or viral pathogens.’
In other words, we cannot prove that the people who get sick and are hospitalized, and very occasionally die, were sickened by a new coronavirus called SARS-CoV-2, nor can we prove that it caused them to develop a new disease called ‘Covid-19.’ It could just as easily be a different virus and a different disease. (And since all the symptoms, including severe pneumonia, correspond seamlessly to what flu can cause historically in vulnerable people… ‘if it looks like a duck and walks like a duck, it is a duck’.
(…..) https://greatreject.org/laboratories-cant-find-covid-19-in-positive-tests/
article source en néerlandais lien hypertexte en bas de l’article
Pour ceux qui veulent traduire https://www.lexilogos.com/anglais_traduction.htm#
« Les procédures de test n’offrent donc aucune signification ni aucun sens. »
Zut alors car on a réalisé pas loin de 77 millions de tests depuis juin 2020 :
https://geodes.santepubliquefrance.fr/#c=home
Il serait intéressant de savoir à qui cela profite-t-il sachant qu’avec un test à 54 euros cela nous donne 4 milliards d’euros que la Sécurité sociale va devoir rembourser. Quand on pense qu’un test ne coûte en réalité qu’un peu plus de 30 centimes !
https://www.google.com/search?client=firefox-b-d&q=prix+d%27un+test+pcr+en+france
Prix dans d’autres pays :
https://img-3.journaldesfemmes.fr/OeHqKSFguenpJ0pTRiiEScrWN-k=/1080x/smart/d302e6f409db43daaa12bc071317845a/ccmcms-jdf/22147707.jpg
S’y ajoute le prix des effets indésirables des vaccins puisqu’il fut décidé de ne pas traiter en amont les positifs !
https://fr.sott.net/article/37096-Bientot-10-000-morts-et-2-millions-d-effets-secondaires-susceptibles-d-etre-lies-aux-vaccins-contre-la-Covid-19
chère Martine, à ce niveau, pour ceux qui pourraient être « intéressés » par l’affaire (Big Pharma…) 1,5 millions d’€ tout de même, c’est juste un pourboire par rapport à un marché juteux en milliards (pas une carrière) juste le prix une (très) belle maison en province, ( ça dépend où, même pas une rente, un ruissellement dans le langage du premier de cordée E. Macron…
il me semble » très simplement » que nous ne pouvons pas compter sur les Labos, les Autorités pour y voir plus clair… mais que sur des compétences indépendantes, comme celle de l’Aimsib et de ses réseaux qui se tricotent tout doucement à l’international.
Aucune raison de désespérer à ce stade…
Voilà si je peux par avance vous envoyer un brin d’optimisme, en attendant le muguet
Imaginons une pandémie internationale qui tue des centaines de milliers de personnes à travers le monde et qu’un vaccin miraculeux ait été trouvé permettant de sauver la planète. L’OMS laisserait les pays dits « riches » payer le développement du produit et permettrait ensuite à ce que les pays dits « pauvres » puissent le fabriquer sans avoir à en payer le brevet. Cette condition est évidemment nécessaire s’il y a péril en la demeure. Le grand philanthrope Bill Gates qui ne paye pas d’impôts grâce à sa fondation, qui arrose généreusement les média, les labos et l’Imperial College pour ses statistiques, serait le premier à épauler cette initiative nommée « open vaccine ».
Qu’en est-il réellement ? Eh bien Bill Gates préfère privilégier les droits de propriété intellectuelle des grandes entreprises pharmaceutiques au détriment de l’accès à des vaccins abondants et bon marché dans le monde en développement.
https://www.aubedigitale.com/bill-gates-confirme-son-opposition-au-mouvement-open-vaccine/
Pourtant un nombre croissant de législateurs démocrates, de groupes de la société civile, de 60 anciens chefs d’État et de 100 lauréats du prix Nobel ont exhorté M. Biden à soutenir cette dérogation.
Moralité de l’histoire, l’argent prime avant tout. Quand on pense que Gates était prêt à sacrifier les boeufs qui pêtaient un peu trop (CO2) pour le bien de l’humanité ! N’y aurait-il pas là aussi une histoire sonnante et trébuchante ? De même qu’avec le réchauffement climatique, cette histoire de pandémie semble être un outil de contrôle des populations. C’est une mise en place d’une dictature mondiale. Le communisme international s’y était essayé mais en échouant. Arrive aujourd’hui les globalistes que Soljenitsyne avait prédits.
@ Bruno
Oui je partage tout à fait l’avis de Philippe Guillemant (Docteur et ingénieur physicien, spécialiste d’Intelligence Artificielle exerçant au CNRS) la finalité n’est pas le vaccin, mais l’économie numérique, et tous ces déploiements et « ruissellements » possibles. On comprend alors mieux les immenses intérêts sous-jacents, tant financiers que de domination néo-coloniale, que permettent l’avance technologique et les brevets.
Par analogie, en regardant le passé, sans les bateaux à vapeur (steam ship), navires motorisés, tout début XIX° siècle pas de Canal de Suez (1869), ou de Panama (1914), et cette avancée technologique, purement matérialiste, a façonné l’histoire pour le meilleur comme pour le pire dans la région.
Et Philippe Guillemant ajoute avec une note d’optimisme (que je partage) :
» Il est en effet peu probable que l’on oblige chaque citoyen à porter une identité numérique lors de ses déplacements si 50% de la population n’est pas vaccinée, car on ne va pas limiter à ce point la liberté de circulation. Par contre, si seulement 5% de la population n’est pas vaccinée, il est fort probable qu’on entrera dans ce nouveau monde.
Donc, je le répète, nous ne sommes pas confrontés à un problème sanitaire avec le virus. Ce problème-là est peanuts à coté du choix de société qui se trouve devant nous, qu’une politique de gouvernance mondiale semble avoir déjà fait à notre place.
Mais je le répète une fois de plus, mon avis est qu’on n’entrera pas dans ce nouveau monde. »
Derrière ces histoires de vaccins, c’est aussi le choix d’une société de demain…
Un mot sur le canal de Panama. L’échec de Ferdinand de Lesseps fut provoqué par la fièvre jaune qui décimait les équipes, ce qui le contraignit d’abandonner. Quand les Américains reprirent le projet ils commencèrent par nettoyer la région des moustiques en faisant bruler du pétrole sur toutes les flaques d’eau, ce qui détruisit les larves. A l’époque le vaccin contre la fièvre jaune n’existait pas.
Difficile de donner du sens à ce qui en a peu, ce qui me paraît vrai tant pour les tests que pour les virus en général, >>> d’après ce que j’en comprends… <<<
De la virologie à l'immunologie, il y a un espace sidéral entre les deux, ce qui fait qu'aucun virus ne peut satisfaire les postulats de Koch (1884), son génome être isolé, cultivé.
Wikipedia est assez explicite, voir l'évolution de ces concepts depuis le XIX° siècle:
"En 2006 des postulats de Koch ont été proposés pour les maladies à protéines infectieuses22.
Dans les années 2010, de nouvelles techniques de bioinformatique, comme le séquenceur d'ADN, conduisent à une nouvelle discipline la métagénomique, qui permet l'identification de l'ADN total d'un échantillon environnemental (par exemple, microbiote intestinal). Cette discipline discute de critères adaptés de causalité, dits « postulats métagénomiques de Koch »23. "
https://fr.wikipedia.org/wiki/Postulats_de_Koch
Et donc ce que l'on sait "sans certitudes", ou comprend des virus ne découle que d'une représentation bioinformatique, et métagénomique.
https://fr.wikipedia.org/wiki/Bio-informatique
https://fr.wikipedia.org/wiki/M%C3%A9tag%C3%A9nomique
Ce qui nous rappelle à l'esprit que la biologie est une science molle et qu'elle patauge dans un relativisme épistémologique adossée depuis peu à des algorithmes. Et nous, notre défaut par méconnaissances nous pataugeons encore dans des représentations pasteuriennes éculées des microbes, à les voir comme agent causal, sans envisager comme Peter Duesberg avec le Sida, que ce que l'on nomme virus ne sont peut-être que des conséquences (de poppers ayant des effets immunosuppresseurs dans le cas du Sida)
https://fr.wikipedia.org/wiki/Relativisme#Relativisme_%C3%A9pist%C3%A9mologique
Au plaisir de lire une réponse à ce commentaire et de me rectifier si j'ai écrit des bêtises
C’est exactemente ce que je pense. A vouloir tout informatiser, le monde va se perdre en omettant la seule chose qui n’autorise que très peu de relativisme : la clinique !
Ce n’est peut-être pas la bonne place dans ce blog mais :
https://smaer.fr/
https://smaer.fr/soutien-au-dr-gerard-maudrux/
https://smaer.fr/lineptie-de-nos-instances-sanitaires-confirmee-par-lordre/
l’offensive vient par le Sud.
Panorama complet de la résistance mondiale dans le dernier livre de Perronne ( »Décidément, ILS n’ont toujours rien compris », avril 2021) avec plein d’autres nouvelles délectables. C’est un très grand bonhomme, indulgent et pas rancunier malgré tout.
Ma question : comment détectent-ils les variants ?
Une personne compétente (virologue) m’a dit qu’on faisait du multiplexage, à savoir, si j’ai bien compris, qu’on rajoutait des amorces.
Mais dans ce cas, on fait fi de la définition première du Covid-19 ! Quelle est cette bouillie ? Expliquez-moi !
https://youtu.be/JsB0muUSEkU
Dr Louis Fouché : « Ici et maintenant »
J’interviens pour Réinfocovid Lundi 3 Mai à 21h avec Jérémie Mercier dans une webconférence en direct « qui s’intitule Covid-19 et thérapeutiques immunitaires », qu’est-ce qu’il faut pas écrire comme c… pour ne pas se faire censurer en quelques minutes par YouTube et consort…
Et n’hésitez pas à parler de la grande générosité de la Belgique envers l’Inde puisqu’elle lui a offerte 9.000 boites de Remdesevir pour lutter contre le coronavirus !
https://www.rtbf.be/info/societe/detail_la-belgique-envoie-des-milliers-de-flacons-de-remdesivir-en-inde-un-medicament-considere-comme-inefficace?id=10752447
Comme quoi la grande philanthropie de Bill Gates fait tâche (d’huile). Cela va rappeler à certains une autre grande générosité concernant les vaccins contre le H1N1 qui ne fonctionnaient pas mais qui furent pourtant expédiés en RDC ! Vive les pays d’Europe et leur sens du partage ! Quand on pense que d’autres les traitent de satanisme !
Le mouton a craint le loup toute sa vie, mais c’est le berger qui l’a mangé !
Proverbe géorgien.
Je vois (je peux me tromper) deux (très) graves inconvénients à un projet d’obligation vaccinale, un mineur, et un majeur.
Le premier ne frappant (comme pour chaque vaccination) qu’un faible, ou très faible % d’individus qui se retrouveraient handicapés, ou décédés, % acceptable du point de vue de la pensée utilitariste qui vise « le bien » du plus grand nombre… laquelle n’étant pas une maïeutique ne mérite pas le nom de philosophie.
Le second, bien plus grave, d’ordre anthropologique inédit dans l’histoire de l’humanité, voire anthroposophique pour d’autres, d’une rupture anthropologique qui frapperait tout le monde, l’humanité entière peut-être (?) si l’on en croit le mage Bill Gates, à savoir qu’il nous faudrait (sur la base d’un dogme) admettre une faiblesse, ou tare, congénitale d’une insuffisance (immunitaire) biologique à pouvoir nous défendre contre ce qui fait partie de la Vie même (Nature diront certains).
Il va de soi que cette option nous ramènerait à n’être que des légumes biologiques, faisant abstraction de toutes considérations holistiques, en nous faisant sombrer dans le réductionnisme scientifique (1), voire bien pire dans le physicalisme (2) qui n’a que faire de considérations holistiques, ou cliniques.
Bref dans les délires de la pensée positiviste, matérialiste..
Il faudrait donc suivant cette pensée en vogue, à chaque nouvel être humain de passer sur les fonds baptismaux pour y recevoir l’onction vaccinale, (supposée) necéssaire à sa survie. Là nous atteignons le fond des délires de la pensée darwiniste, qui est, on le sait moins, tant eugéniste que raciste à la base.
Dans cette situation indécise, cornélienne pour certains, le problème est que NOUS NE SOMMES PAS QUE DE LA BIDOCHE (des cobayes)… nous serions mus par « une énergie », des champs énergétiques, (erratiques ? ou browniens ? peu importe à ce stade de méconnaissances) comme n’importe quel atome, ce que la science préfère ne pas voir… ou ne pas prendre en considération
Le résultat étant de nous « objetiser »…numériser…
(1) https://fr.wikipedia.org/wiki/R%C3%A9ductionnisme
(2) https://fr.wikipedia.org/wiki/Physicalisme
Jai parcouru les commentaires, je ne trouve quasiment personne répondant clairement à la question: le virus a t il été isolé et purifié et cultivé ? J ai l’impression d’avoir compris que il s agit plutôt d’une reconstitution bio-informatique:
« De la virologie à l’immunologie, il y a un espace sidéral entre les deux, ce qui fait qu’aucun virus ne peut satisfaire les postulats de Koch (1884), son génome être isolé, cultivé.
Wikipedia est assez explicite, voir l’évolution de ces concepts depuis le XIX° siècle:
« En 2006 des postulats de Koch ont été proposés pour les maladies à protéines infectieuses22.
Dans les années 2010, de nouvelles techniques de bioinformatique, comme le séquenceur d’ADN, conduisent à une nouvelle discipline la métagénomique, qui permet l’identification de l’ADN total d’un échantillon environnemental (par exemple, microbiote intestinal). Cette discipline discute de critères adaptés de causalité, dits « postulats métagénomiques de Koch »2 »
Si quelq’un pouvait être encore plus clair que Njama et pouvoir le vulgariser….. J’en demande trop peut être ?